公司新聞
香港,2023年8月16日
億勝生物科技有限公司(“億勝生物”或“集團(tuán)”;股份代碼:1061.HK)今日公布截至2023年6月30日止(“回顧期內(nèi)”)的中期財(cái)務(wù)業(yè)績。
財(cái)務(wù)表現(xiàn)恢復(fù)至COVID-19前的正常營運(yùn)水平
于回顧期內(nèi),集團(tuán)實(shí)現(xiàn)整體收入約8.99億港元,較去年同期增長37.1%,顯示業(yè)務(wù)恢復(fù)至COVID-19前的正常營運(yùn)水平。集團(tuán)的凈利潤較去年同期約1.39億港元增長22.0%至約1.70億港元。
截至2023年6月30日,集團(tuán)的現(xiàn)金及現(xiàn)金等值物約5.06億港元(2022年12月31日:約5.43億港元)。董事會(huì)欣然建議派發(fā) 2023年中期股息每股普通股 0.045港元(截至 2022年 6月 30日止六個(gè)月:0.04港元)。
眼科及外科分部收入增加
集團(tuán)收入主要由眼科及外科(創(chuàng)傷修復(fù))兩部分組成,其中眼科收入同比增長41.6%至約3.82億港元,占集團(tuán)收入的42.4%;外科收入同比增長34.0%至約5.18億港元,占集團(tuán)收入的57.6%。目前具有增長動(dòng)力的核心產(chǎn)品為:
1. 眼科-貝復(fù)舒®系列(貝復(fù)舒®滴眼液、貝復(fù)舒®眼用凝膠及貝復(fù)舒®單劑量滴眼液)、妥布霉素滴眼液、左氧氟沙星滴眼液、玻璃酸鈉滴眼液及適麗順®(卵磷脂絡(luò)合碘膠囊);
2. 外科(創(chuàng)傷護(hù)理修復(fù))-貝復(fù)濟(jì)®系列(貝復(fù)濟(jì)®液體制劑、貝復(fù)濟(jì)®凍干粉及貝復(fù)新®凝膠)、Carisolv®齲齒凝膠、伢典醫(yī)生®漱口水、伊血安顆粒及皮耐克®可吸收性敷料。
重大業(yè)務(wù)進(jìn)展
集團(tuán)致力于務(wù)實(shí)投入新產(chǎn)品及技術(shù)以強(qiáng)化產(chǎn)品及研發(fā)管線,作為眼科近中期增長動(dòng)力及腫瘤科新治療領(lǐng)域的長期計(jì)劃。目前處于臨床開發(fā)后期階段的眼科產(chǎn)品的主要投資概述如下:
繼收購SkQ1相關(guān)的知識(shí)產(chǎn)權(quán)后,正重新建立VISTA計(jì)劃
為了使集團(tuán)于干眼癥領(lǐng)域的美國藥監(jiān)局VISTA計(jì)劃的持續(xù)發(fā)展更具靈活性及獨(dú)立性,并使集團(tuán)能夠進(jìn)一步探索開發(fā)其他適應(yīng)癥的眼科產(chǎn)品,集團(tuán)自Mitotech成功獲得眼科領(lǐng)域與SkQ1相關(guān)的專利及專有技術(shù)許可協(xié)議及專利轉(zhuǎn)讓契據(jù)。
繼2022年10月收購與SkQ1相關(guān)的知識(shí)產(chǎn)權(quán)后,本集團(tuán)的首要任務(wù)為完成SkQ1的化學(xué)成分生產(chǎn)與控制(CMC)、專有技術(shù)及知識(shí)產(chǎn)權(quán)的轉(zhuǎn)讓。同時(shí),本集團(tuán)正在與監(jiān)管機(jī)構(gòu)重新建立VISTA計(jì)劃,以在繼續(xù)進(jìn)行臨床試驗(yàn)前減輕任何可識(shí)別的風(fēng)險(xiǎn)。根據(jù)弗若斯特沙利文的資料,2020年中國境內(nèi)僅中度至重度干眼癥患者人數(shù)逾1.2億。SkQ1產(chǎn)品的潛在市場(chǎng)規(guī)模巨大。
EB12-20145P (HLX04-O)全球三期臨床研究取得重大進(jìn)展
2020年,集團(tuán)與上海復(fù)宏漢霖生物技術(shù)股份有限公司訂立共同開發(fā)及獨(dú)家許可協(xié)議,共同開發(fā)一種用于治療滲出性(濕性)年齡相關(guān)性黃斑變性(“濕性AMD”)的重組抗血管內(nèi)皮生長因子(“抗VEGF”)人源化單克隆抗體注射液EB12-20145P。于回顧期內(nèi),該產(chǎn)品已獲批準(zhǔn)在澳大利亞、美國、新加坡、俄羅斯、塞爾維亞以及匈牙利、西班牙、拉脫維亞、捷克共和國及波蘭等歐盟國家開展三期臨床試驗(yàn)。截至目前,用以治療濕性AMD的EB12-20145P于中國、拉脫維亞、澳大利亞及美國的三期臨床研究已先后完成首例患者給藥。此外,用以治療濕性AMD之EB12-20145P的1/2期臨床研究已顯示其安全性及耐受性良好,并展現(xiàn)出初步療效。
2023年2月,本集團(tuán)與復(fù)宏漢霖訂立一份經(jīng)修訂協(xié)議,以修訂共同開發(fā)許可協(xié)議的若干條款,其中包括支付監(jiān)管及商業(yè)銷售里程碑的付款以及開發(fā)成本。詳細(xì)信息已于2023年2月22日的公司公告和2023年3月8日的公司年度業(yè)績公告中公布。
抗VEGF許可產(chǎn)品可用于治療濕性AMD、糖尿病性黃斑水腫、視網(wǎng)膜靜脈阻塞引起的黃斑水腫及近視性黃斑部病變。根據(jù)弗若斯特沙利文的資料,中國境內(nèi)該等4類病患人數(shù)于2020年估計(jì)超逾1580萬人。假設(shè)每病患于治療的首年注射4個(gè)劑量并于其后年度注射2至3個(gè)劑量,抗VEGF許可產(chǎn)品的潛在市場(chǎng)規(guī)模巨大。
2023年獲得的榮譽(yù)及獎(jiǎng)項(xiàng)
集團(tuán)全資附屬公司珠海億勝生物制藥有限公司榮登2022年珠海市創(chuàng)新百強(qiáng)企業(yè)創(chuàng)新綜合實(shí)力100強(qiáng)和2022年度TOP100中國化藥企業(yè)。同時(shí),集團(tuán)的貝復(fù)舒已連續(xù)五年榮登中國醫(yī)藥品牌榜,證明業(yè)界對(duì)集團(tuán)旗艦生物藥的療效及質(zhì)量的認(rèn)可。
市場(chǎng)開發(fā)鞏固市場(chǎng)渠道能力
數(shù)年來,集團(tuán)一直不懈投入資源積蓄及強(qiáng)化其市場(chǎng)渠道能力。截至2023年6月30日,集團(tuán)于中國設(shè)有43間銷售推廣辦事處,共有逾1,200名銷售代表,覆蓋中國主要省份、城市及縣城逾12,100家醫(yī)院及醫(yī)療機(jī)構(gòu)以及逾2,100家藥房。在渠道下沉,開發(fā)多線城市市場(chǎng)的同時(shí),通過在線醫(yī)療咨詢和電子處方平臺(tái),為慢性病患者提供更多服務(wù)。
自2020年以來,集團(tuán)通過新加坡基地向東南亞國家擴(kuò)大市場(chǎng)準(zhǔn)入,取得了良好的發(fā)展勢(shì)頭。
研究與開發(fā)
于回顧期內(nèi),集團(tuán)將繼續(xù)專注于執(zhí)行其5年(2021年至2025年)研發(fā)發(fā)展計(jì)劃。截至報(bào)告日期,共有16項(xiàng)研發(fā)計(jì)劃處于臨床前至臨床階段,其中下列4項(xiàng)眼科計(jì)劃處于后期臨床階段,被視為中期增長動(dòng)力:
億勝生物科技有限公司(“億勝生物”或“集團(tuán)”;股份代碼:1061.HK)今日公布截至2023年6月30日止(“回顧期內(nèi)”)的中期財(cái)務(wù)業(yè)績。
財(cái)務(wù)表現(xiàn)恢復(fù)至COVID-19前的正常營運(yùn)水平
于回顧期內(nèi),集團(tuán)實(shí)現(xiàn)整體收入約8.99億港元,較去年同期增長37.1%,顯示業(yè)務(wù)恢復(fù)至COVID-19前的正常營運(yùn)水平。集團(tuán)的凈利潤較去年同期約1.39億港元增長22.0%至約1.70億港元。
截至2023年6月30日,集團(tuán)的現(xiàn)金及現(xiàn)金等值物約5.06億港元(2022年12月31日:約5.43億港元)。董事會(huì)欣然建議派發(fā) 2023年中期股息每股普通股 0.045港元(截至 2022年 6月 30日止六個(gè)月:0.04港元)。
眼科及外科分部收入增加
集團(tuán)收入主要由眼科及外科(創(chuàng)傷修復(fù))兩部分組成,其中眼科收入同比增長41.6%至約3.82億港元,占集團(tuán)收入的42.4%;外科收入同比增長34.0%至約5.18億港元,占集團(tuán)收入的57.6%。目前具有增長動(dòng)力的核心產(chǎn)品為:
1. 眼科-貝復(fù)舒®系列(貝復(fù)舒®滴眼液、貝復(fù)舒®眼用凝膠及貝復(fù)舒®單劑量滴眼液)、妥布霉素滴眼液、左氧氟沙星滴眼液、玻璃酸鈉滴眼液及適麗順®(卵磷脂絡(luò)合碘膠囊);
2. 外科(創(chuàng)傷護(hù)理修復(fù))-貝復(fù)濟(jì)®系列(貝復(fù)濟(jì)®液體制劑、貝復(fù)濟(jì)®凍干粉及貝復(fù)新®凝膠)、Carisolv®齲齒凝膠、伢典醫(yī)生®漱口水、伊血安顆粒及皮耐克®可吸收性敷料。
重大業(yè)務(wù)進(jìn)展
集團(tuán)致力于務(wù)實(shí)投入新產(chǎn)品及技術(shù)以強(qiáng)化產(chǎn)品及研發(fā)管線,作為眼科近中期增長動(dòng)力及腫瘤科新治療領(lǐng)域的長期計(jì)劃。目前處于臨床開發(fā)后期階段的眼科產(chǎn)品的主要投資概述如下:
繼收購SkQ1相關(guān)的知識(shí)產(chǎn)權(quán)后,正重新建立VISTA計(jì)劃
為了使集團(tuán)于干眼癥領(lǐng)域的美國藥監(jiān)局VISTA計(jì)劃的持續(xù)發(fā)展更具靈活性及獨(dú)立性,并使集團(tuán)能夠進(jìn)一步探索開發(fā)其他適應(yīng)癥的眼科產(chǎn)品,集團(tuán)自Mitotech成功獲得眼科領(lǐng)域與SkQ1相關(guān)的專利及專有技術(shù)許可協(xié)議及專利轉(zhuǎn)讓契據(jù)。
繼2022年10月收購與SkQ1相關(guān)的知識(shí)產(chǎn)權(quán)后,本集團(tuán)的首要任務(wù)為完成SkQ1的化學(xué)成分生產(chǎn)與控制(CMC)、專有技術(shù)及知識(shí)產(chǎn)權(quán)的轉(zhuǎn)讓。同時(shí),本集團(tuán)正在與監(jiān)管機(jī)構(gòu)重新建立VISTA計(jì)劃,以在繼續(xù)進(jìn)行臨床試驗(yàn)前減輕任何可識(shí)別的風(fēng)險(xiǎn)。根據(jù)弗若斯特沙利文的資料,2020年中國境內(nèi)僅中度至重度干眼癥患者人數(shù)逾1.2億。SkQ1產(chǎn)品的潛在市場(chǎng)規(guī)模巨大。
EB12-20145P (HLX04-O)全球三期臨床研究取得重大進(jìn)展
2020年,集團(tuán)與上海復(fù)宏漢霖生物技術(shù)股份有限公司訂立共同開發(fā)及獨(dú)家許可協(xié)議,共同開發(fā)一種用于治療滲出性(濕性)年齡相關(guān)性黃斑變性(“濕性AMD”)的重組抗血管內(nèi)皮生長因子(“抗VEGF”)人源化單克隆抗體注射液EB12-20145P。于回顧期內(nèi),該產(chǎn)品已獲批準(zhǔn)在澳大利亞、美國、新加坡、俄羅斯、塞爾維亞以及匈牙利、西班牙、拉脫維亞、捷克共和國及波蘭等歐盟國家開展三期臨床試驗(yàn)。截至目前,用以治療濕性AMD的EB12-20145P于中國、拉脫維亞、澳大利亞及美國的三期臨床研究已先后完成首例患者給藥。此外,用以治療濕性AMD之EB12-20145P的1/2期臨床研究已顯示其安全性及耐受性良好,并展現(xiàn)出初步療效。
2023年2月,本集團(tuán)與復(fù)宏漢霖訂立一份經(jīng)修訂協(xié)議,以修訂共同開發(fā)許可協(xié)議的若干條款,其中包括支付監(jiān)管及商業(yè)銷售里程碑的付款以及開發(fā)成本。詳細(xì)信息已于2023年2月22日的公司公告和2023年3月8日的公司年度業(yè)績公告中公布。
抗VEGF許可產(chǎn)品可用于治療濕性AMD、糖尿病性黃斑水腫、視網(wǎng)膜靜脈阻塞引起的黃斑水腫及近視性黃斑部病變。根據(jù)弗若斯特沙利文的資料,中國境內(nèi)該等4類病患人數(shù)于2020年估計(jì)超逾1580萬人。假設(shè)每病患于治療的首年注射4個(gè)劑量并于其后年度注射2至3個(gè)劑量,抗VEGF許可產(chǎn)品的潛在市場(chǎng)規(guī)模巨大。
2023年獲得的榮譽(yù)及獎(jiǎng)項(xiàng)
集團(tuán)全資附屬公司珠海億勝生物制藥有限公司榮登2022年珠海市創(chuàng)新百強(qiáng)企業(yè)創(chuàng)新綜合實(shí)力100強(qiáng)和2022年度TOP100中國化藥企業(yè)。同時(shí),集團(tuán)的貝復(fù)舒已連續(xù)五年榮登中國醫(yī)藥品牌榜,證明業(yè)界對(duì)集團(tuán)旗艦生物藥的療效及質(zhì)量的認(rèn)可。
市場(chǎng)開發(fā)鞏固市場(chǎng)渠道能力
數(shù)年來,集團(tuán)一直不懈投入資源積蓄及強(qiáng)化其市場(chǎng)渠道能力。截至2023年6月30日,集團(tuán)于中國設(shè)有43間銷售推廣辦事處,共有逾1,200名銷售代表,覆蓋中國主要省份、城市及縣城逾12,100家醫(yī)院及醫(yī)療機(jī)構(gòu)以及逾2,100家藥房。在渠道下沉,開發(fā)多線城市市場(chǎng)的同時(shí),通過在線醫(yī)療咨詢和電子處方平臺(tái),為慢性病患者提供更多服務(wù)。
自2020年以來,集團(tuán)通過新加坡基地向東南亞國家擴(kuò)大市場(chǎng)準(zhǔn)入,取得了良好的發(fā)展勢(shì)頭。
研究與開發(fā)
于回顧期內(nèi),集團(tuán)將繼續(xù)專注于執(zhí)行其5年(2021年至2025年)研發(fā)發(fā)展計(jì)劃。截至報(bào)告日期,共有16項(xiàng)研發(fā)計(jì)劃處于臨床前至臨床階段,其中下列4項(xiàng)眼科計(jì)劃處于后期臨床階段,被視為中期增長動(dòng)力:
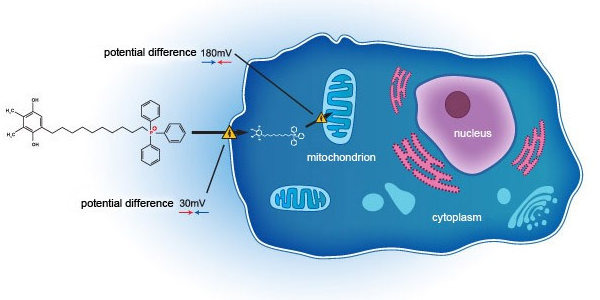
- EB11-18136P:SkQ1滴眼液,三期臨床第二階段試驗(yàn)(VISTA-2)頂線數(shù)據(jù)已于2021年2月24日發(fā)布(美國藥監(jiān)局)
- EB11-15120P:阿奇霉素滴眼液,外部專家正在審查(中國國家藥品監(jiān)督管理局)
- EB12-20145P:貝伐珠單抗(用于治療濕性年齡相關(guān)性黃斑變性),三期臨床試驗(yàn)(美國藥監(jiān)局、歐洲藥品管理局、澳大利亞藥物管理局及中國國家藥品監(jiān)督管理局)
- EB11-21148P:環(huán)孢素滴眼液,二期臨床試驗(yàn)(中國國家藥品監(jiān)督管理局)
集團(tuán)持有73份專利證書或授權(quán)書,包括52項(xiàng)發(fā)明專利、14項(xiàng)實(shí)用新型專利及7項(xiàng)外觀專利。同時(shí),本集團(tuán)目前已將其研發(fā)資源多元化至珠海(中國)、波士頓(美國)、倫敦(英國)及新加坡的多個(gè)研究基地,這既能支持集團(tuán)對(duì)新療法的追求,也能支持我們對(duì)全球人才的獲取。
億勝生物科技主席嚴(yán)名熾先生表示: “憑借著韌性與實(shí)力,我們很高興能將集團(tuán)的業(yè)務(wù)表現(xiàn)恢復(fù)到 COVID-19 前的正常營運(yùn)水準(zhǔn)。除去不可預(yù)測(cè)的情況外,集團(tuán)將基于優(yōu)異的發(fā)展韌性與優(yōu)勢(shì)的市場(chǎng)地位,蓄勢(shì)增長,對(duì)取得持續(xù)成果持樂觀態(tài)度。
謹(jǐn)借此機(jī)會(huì)向集團(tuán)所有股東、業(yè)務(wù)伙伴及客戶致以衷心謝意,感謝各位對(duì)集團(tuán)的信任、支持及與我們衷誠合作,并感謝每一位成員作出的不懈努力,致力將公司打造為一家銳意進(jìn)取且前途光明的制藥企業(yè)。”
~完~
關(guān)于億勝生物 (股票代碼﹕1061)
億勝生物科技有限公司是一間專注于研發(fā),生產(chǎn)和銷售基因工程藥物b-bFGF(FGF-2)的生物制藥企業(yè),自1998年起已有六種基因工程藥物在中國上市銷售。此外,公司還擁有一系列不含防腐劑單劑量滴眼液和適麗順®卵磷脂絡(luò)合碘膠囊等產(chǎn)品。公司產(chǎn)品主要應(yīng)用于眼科及皮膚科處方藥領(lǐng)域的創(chuàng)傷修復(fù)及疾病治療,目前憑借在中國主要城市的43個(gè)銷售推廣辦事處已成功覆蓋中國逾12,100家醫(yī)院。公司依托自身在生長因子和抗體領(lǐng)域的研發(fā)平臺(tái),擁有多個(gè)臨床階段的項(xiàng)目,涵蓋廣泛的領(lǐng)域和適應(yīng)癥。
























































 粵公網(wǎng)安備 44049102496184號(hào)
粵公網(wǎng)安備 44049102496184號(hào)